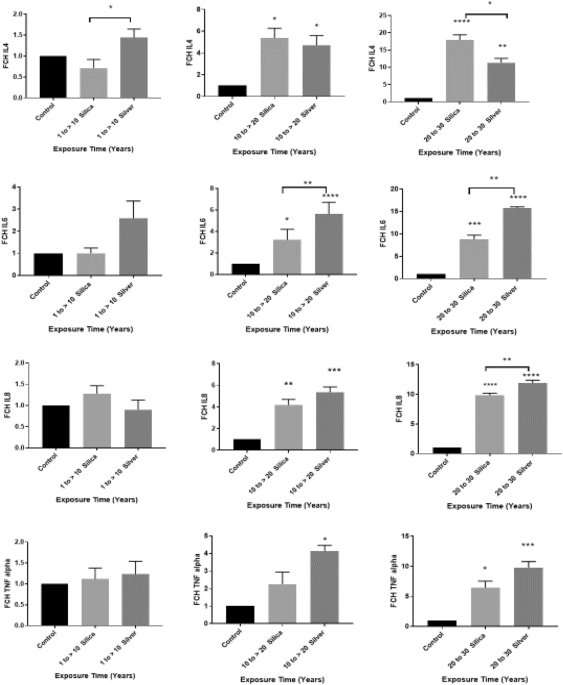
銀およびシリカのナノ粒子への慢性的な曝露により、皮膚病変を発症した労働者のIL8、TNF-α、IL4およびIL6の遺伝子発現が顕著に増加した
倍率変化(FCH)として表されるPCR結果は、職場で銀およびシリカのナノ粒子に長時間曝露された後に皮膚病変を発症した参加者では、健康な参加者と比較して、IL8、TNF-α、IL4、およびIL6のmRNAレベルが顕著に上方制御されていたことを示した。ナノ粒子に曝露されなかった対照者。 銀ナノ粒子への曝露は、2回または3回の曝露後にIL8、TNF-α、IL4およびIL6の遺伝子発現を有意に上昇させた(IL8についてはP < 0.001、TNF-αについてはP < 0.05、IL6についてはP < 0.0001、IL4についてはP < 0.05)。 (IL8 については P < 0.0001、TNF-α については P < 0.0001、IL4 については P < 0.01、IL6 については P < 0.0001) 数十年の曝露。 同様に、シリカナノ粒子への曝露は、曝露から 20 年 (P < 0.01) および 30 年 (P < 0.0001) 後に、IL8 の遺伝子発現を有意に上昇させました。 シリカナノ粒子への曝露は、30 年間の曝露後にのみ TNF-α レベルの有意な増加をもたらしました (P < 0.05)。 さらに、IL8レベルは、シリカナノ粒子に曝露された人々と比較して、銀ナノ粒子に曝露された人々において有意に高かった(P < 0.01)。 同様に、シリカナノ粒子への曝露は、20年(P<0.05)または30年(IL4についてはP<0.0001、IL6についてはP<0.001)の曝露後、IL4およびIL6の遺伝子発現を有意に上昇させた。 IL6レベルは、シリカナノ粒子に曝露された患者と比較して、銀ナノ粒子に曝露された患者の方が有意に高かった(P < 0.01)。 曝露から最初の10年間では、銀ナノ粒子を投与された人のIL4レベルは有意に(P < 0.05)高かったが、曝露から30年後にはシリカナノ粒子を投与された人のIL4レベルは顕著に(P < 0.05)高かった(図1)。 1)。 銀およびシリカのナノ粒子に曝露された作業員は、30 年間の曝露後に IL8、TNF-α、IL4、および IL6 の mRNA レベルが数倍高くなり、彼らの遺伝子発現は曝露期間が数十年になるにつれて継続的に増加しました(図 2)。
銀およびシリカのナノ粒子への長期曝露後に皮膚病変を発症した作業員におけるIL8、TNF-α、IL4およびIL6の遺伝子発現。 参加者は曝露の長さに基づいて分けられました。 IL8、TNF-α、IL4、およびIL6の遺伝子発現を、ナノ粒子への曝露のない健康な対照群と、銀およびシリカのナノ粒子への長期曝露後に皮膚病変を発症した作業員との間で比較した。 スチューデントのt検定を使用して、対照群と各ナノ粒子群とを比較するか、またはナノ粒子群を相互に比較した。 *P < 0.05、**P < 0.01、***P < 0.001、****P < 0.0001。 データは平均値 ± SD として表示されます。
IL8、TNF-α、IL4、およびIL6の遺伝子発現は、銀およびシリカのナノ粒子への数十年の曝露に基づいています。 IL8、TNF-α、IL4、およびIL6の遺伝子発現を、暴露期間が異なる群間で比較した。 スチューデントのt検定を使用して、対照群と各ナノ粒子群とを比較するか、またはナノ粒子群を相互に比較した。 *P < 0.05、**P < 0.01、***P < 0.001、****P < 0.0001。 データは平均値 ± SD として表示されます。
CRP検査
C 反応性タンパク質は重症度の基準として使用され、すべてのサンプルで炎症が示され、2 つの陽性 (++) によりリアルタイム PCR 結果が確認されました。
ネットワーク薬理調査
Network Pharmacology Surveyのグラフは、IL4、IL6、IL8、TNFαなどのさまざまな遺伝子の発現に対するシリカおよび銀ナノ粒子の影響が、アトピー性皮膚炎などのさまざまな皮膚疾患の発生につながることを示しています。 これは人間のサンプルに関する私たちの調査と一致しています(図2)。 3)。
ネットワーク薬理学調査のグラフと、ネットワーク薬理学の疾患関連の解釈。
図では、 3ネットワーク薬理学の疾患関連解釈では、発疹は IL4 レベルの上昇と有意な関連性はありませんでしたが、皮膚の乾燥は IL4 レベルの上昇と有意に関連しています。
シリカおよびシルバー関連遺伝子は、最近の論文の包括的な文献レビューを通じて厳選されました。 その後、シリカと銀に関連する 4 つの特定のターゲット (IL4、IL6、IL8、および TNF) を特定しました。 私たちはそれらを DisGeNET オンライン データベース内の検索に使用しました (https://www.disgenet.org/; 2023 年 10 月 11 日にアクセス)「GDA スコア ≥ 0.4」のフィルタリング基準を使用して、潜在的な疾患の関連性を明らかにします。 すべての皮膚系関連疾患は手動で選択され、Cytoscape 10.1 を使用してネットワーク薬理学グラフが構築されました。11。
統計調査
人口統計の比較
ナノ粒子への曝露時間が異なる対照群と症例群における年齢や性別などの人口統計学的要因は、統計的には差がありませんでした。
暴露期間(数十年)と症状の発現との関連性
フィッシャーの正確確率検定では、暴露期間と血圧、咳、喉の痛み、呼吸困難、喘鳴、脱毛、発汗、皮膚刺激、皮膚の色白化との間に有意な関連性は見られなかったが、暴露期間の長さは有意に関連していたことが明らかになった。くしゃみを伴う (P < 0.001)、薄片状の皮膚 (P < 0.002)、皮膚の荒れ (P < 0.01)、あかぎれ (P < 0.03)、ほくろ (P < 0.05)、発疹 (P < 0.05)、および皮膚の発赤 (P < 0.05)。
症状とサイトカインレベルの関連性を測定するためのスチューデントの t 検定分析
スチューデントの t 検定分析を実行した後、性別、皮膚の発赤、発疹、脱毛、皮膚の美白、皮膚の炎症、発汗は IL4 レベルと有意な相関関係がないことがわかりましたが、ナノ粒子への曝露 (P < 0.001)、薄片状の皮膚(P < 0.003)、皮膚の荒れ (P < 0.007)、あかぎれ (P < 0.002)、ほくろ (P < 0.048) は、スチューデントの t 検定で IL4 レベルと有意に相関しました。 同様に、性別、皮膚の発赤、あかぎれ、脱毛、皮膚の美白、皮膚の炎症および発汗はIL6レベルと有意な相関を示さなかったが、ナノ粒子曝露(P < 0.001)、薄片状皮膚(P < 0.001)、皮膚の荒れ(P < 0.003)はIL6レベルと有意な相関を示さなかった。 )、発疹(P < 0.014)、ほくろ(P < 0.005)は、スチューデントの t 検定における IL6 レベルの発現と顕著に相関しました。 性別、皮膚の発赤、脱毛、皮膚の美白、皮膚の炎症および発汗は、スチューデントの t 検定における IL8 発現と有意な相関を示さなかったが、ナノ粒子曝露 (P < 0.001)、薄片状の皮膚 (P < 0.001)、皮膚の荒れは、IL8 発現と有意な相関関係を示さなかった。 (P < 0.003)、あかぎれ (P < 0.004)、発疹 (P < 0.014)、ほくろ (P < 0.003) はそれを顕著に上方制御しました。 同様に、性別、皮膚の発赤、脱毛、皮膚の美白、皮膚の炎症、発汗は TNF-α レベルと有意な相関関係がなかったのに対し、ナノ粒子曝露 (P < 0.001)、薄片状の皮膚 (P < 0.001)、皮膚の荒れ (P < 0.001) は TNF-α レベルと有意な相関関係がありませんでした。 0.002)、あかぎれ(P < 0.018)、発疹(P < 0.036)、ほくろ(P < 0.11)は、TNF-α 発現と有意に相関しています。 すべての計算において、この研究の対照群に関して比較が行われました。
1709838060
#産業内で銀およびシリカのナノ粒子に長時間曝露された労働者では炎症性サイトカイン遺伝子の高い発現が検出される可能性がある
2024-03-07 18:38:42