1709394390
2024-03-02 15:38:39
MLはOS患者の予後と関連していた
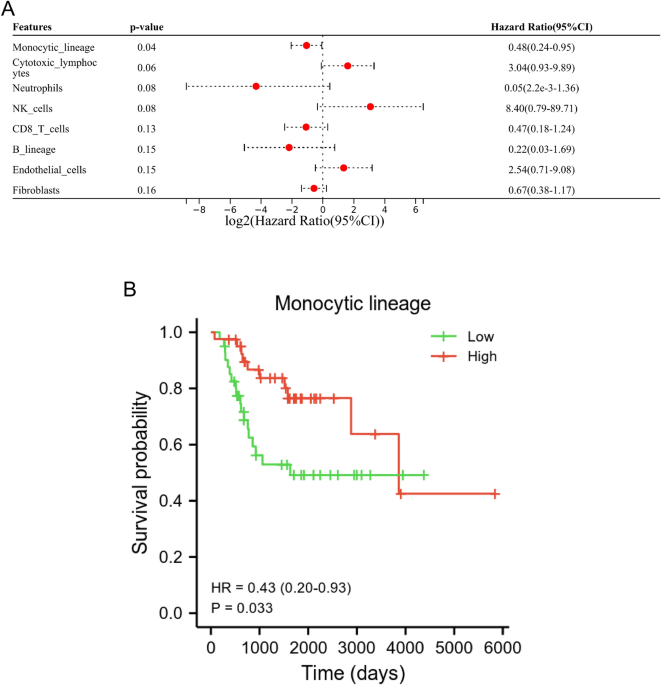
私たちの研究では、MCPカウンターアルゴリズムと単変量および単変量Cox回帰分析を実行して、生存に関連する免疫細胞を特定しました。 単変量コックス回帰分析の結果、ML は OS 患者の生存に関連する免疫細胞であることが示されました (図 1)。 1A)。 さらに、カプラン・マイヤー分析では、低レベルのMLがOS患者の予後不良に関連していることが示されました(p = 0.033、図1)。 1B)。
ML は OS 患者の予後不良に関連していました。 (A) TARGET データベースに基づく 6 つの免疫細胞と 2 つの間質細胞の一変量 Cox 解析。 (B) カプラン・マイヤー分析は、ML のレベルが患者の予後に有意に関連していることを示しました。
DEG と 2 つのサブグループ間の潜在的なシグナル伝達経路の分析
DEG の分析により、合計 435 の DEG が特定されました (図 1)。 2A、B)。 LML と比較して、HML グループでは 101 個の遺伝子が下方制御され、334 個の遺伝子が上方制御されました。 生物学的プロセス (BP) の観点から見ると、これらの DEG は、リンパ球の活性化、T 細胞の活性化、細胞活性化の正の制御、T 細胞の活性化の制御、白血球の細胞間接着などに関与しています。 (CC)、DEG は細胞膜の外側、分泌顆粒膜、フィコリン 1 に富む顆粒、免疫学的シナプス、NADPH オキシダーゼ複合体などに関与していました。分子機能 (MF) の観点から見ると、DEG は炭水化物が著しく豊富でした。結合、サイトカイン受容体結合、サイトカイン結合、サイトカイン受容体活性、C-C ケモカイン受容体活性など。KEGG の用語では、DEG は主に造血細胞系譜、破骨細胞分化、サイトカイン-サイトカイン受容体相互作用、B 細胞受容体シグナル伝達に富んでいました。通路など(図) 3)。
LML サブグループと HML サブグループ間の DEG の識別。 (A) ボルケーノ プロットは、LML サブグループと HML サブグループ間の DEG を示しました。 緑色の点はダウンレギュレートされた遺伝子を表し、一方、赤色のドットはアップレギュレートされた遺伝子を表しました。 (B) ヒートマップ プロットは、LML サブグループと HML サブグループ間の上位 50 DEG を示しています。
DEG の濃縮分析。 (A) バブル プロットは GO と KEGG の結果を示しています。 ネットワーク図は、免疫および炎症に関連する GO-BP 用語 (B) と KEGG 経路 (C) を示しています。 青色のノードは GO-BP 用語または KEGG 経路を表し、赤色のノードはその経路に関与する遺伝子を表しました。
免疫細胞浸潤
OSにおける免疫微小環境を解読するために、LMLサブグループとHMLサブグループ間の免疫状態を分析しました。 図に示すように。 4A、HML グループと比較して、間質スコア、免疫スコア、および ESTIMATE スコアは LML グループで減少しましたが (p < 0.01)、腫瘍純度は LML グループで有意に増加しました (p < 0.01)。 HML グループと比較して、LML グループでは内皮細胞、骨髄樹状細胞、単球系、B 系、T 細胞、CD8 T 細胞のレベルが有意に減少しました (p < 0.05) (図 1)。 4B)。
2 つのサブグループにおける免疫細胞浸潤レベルの状況。 (A) LML サブグループと HML サブグループの間の間質スコア、免疫スコア、ESTIMATE スコア、および腫瘍純度の比較。 (B) LML サブグループと HML サブグループ間の免疫細胞浸潤レベルの比較。 *p < 0.05、**p < 0.01、および ***p < 0.001。
予後リスクモデルの構築と評価
単変量コックス回帰分析の後、122 個の全生存関連遺伝子をスクリーニングしました (表 S1)。 その後、LASSO Cox 回帰分析により、多変量 Cox 回帰分析用の 8 つの遺伝子 (CCDC26、TERT、GJA5、KRT18P28、LILRA6、PDE1B、CD180、および IL2RA) が同定されました (図 1)。 5A、B)。 最後に、3 つの重要な全生存関連遺伝子 (TERT、IL2RA、および CCDC26) がスクリーニングされ、予後モデルを確立するために使用されました (図 1)。 5C)。
ML関連予後モデルの確立。 (A、B) LASSO 回帰分析。 (C) 多変量コックス回帰分析。
TARGET データセットでは、TERT および CCDC26 の発現レベルは低リスク グループで下方制御され、一方、IL2RA の発現は低リスク グループで上方制御されました。 さらに、高リスクグループでは生存率が低かった(図1)。 6A)。 低リスク群の OS 患者は、高リスク群の OS 患者よりも長い全生存期間を示しました(図 2)。 6B、p < 0.001)。 この予後モデルの AUC は 1 年目で 0.8、3 年目で 0.87、5 年目で 0.85 でした (図 1)。 6C)、この結果は、予後モデルが OS 患者に対して良好な診断性能を持っていることを示しました。 また、GSE21257 データセットを使用して、リスク モデルの診断と予後特徴を検証しました。 図に示すように。 7A、TERT および CCDC26 の発現レベルは低リスク グループで下方制御され、一方、IL2RA の発現は低リスク グループで上方制御されました。 さらに、高リスクグループは生存率が低かった。 低リスク群の OS 患者は、高リスク群の OS 患者よりも長い全生存期間を示しました (p = 0.025) (図 1)。 7B)。 この予後モデルの AUC は、1 年目で 0.84、3 年目で 0.67、5 年目で 0.68 でした (図 1)。 7C)。 これらの結果は、TARGET データセットの結果と一致しました。
TARGET データベース内の予後モデルの評価。 (A) TERT、CCDC26、IL2RAの発現レベル(下)、生存状況(中)、および低リスク群と高リスク群間のリスクスコアの分布(上)。 (B) 生存分析により、低リスク群と高リスク群の違いが示されました。 (C) 予後モデルの時間依存 ROC 曲線分析。
GSE21257 データセットの予後モデルの検証。 (A) TERT、CCDC26、IL2RAの発現レベル(下)、生存状況(中)、および低リスク群と高リスク群間のリスクスコアの分布(上)。 (B) 生存分析により、低リスク群と高リスク群の違いが示されました。 (C) 予後モデルの時間依存 ROC 曲線分析。
さらに、OS 患者の予後予測をさらに支援するノモグラムが確立されました (図 1)。 8A)。 ノモグラムの予測結果は、ノモグラム検量線に基づく OS 患者の観察結果と非常に一致していました (図 1)。 8B)。
ノモグラムの確立。 (A) 転移とリスクスコアを使用してノモグラムを確立しました。 (B) ノモグラムの検量線。
予後遺伝子の相互作用解析
GeneMANIA データベースを使用することで、特徴的な遺伝子 (TERT および IL2RA) のタンパク質相互作用ネットワークを構築することに成功しました。 この解析により、特徴遺伝子と相互作用する合計20個の遺伝子を発見しました(図1)。 9A)。 これら 22 個の遺伝子に対して機能強化解析を実施しました。 濃縮分析から得られた結果は、これらの遺伝子が主にテロメア構成、テロメア維持、ヒトT細胞白血病ウイルス1型感染、Th1およびTh2細胞分化などに関連していることを示しました。 9B)。
特徴的な遺伝子の相互作用解析。 (A) シグネチャー遺伝子の共発現ネットワーク。 (B) GO および KEGG による共発現遺伝子の機能濃縮分析。
リスクモデル関連遺伝子と腫瘍微小環境(TME)との関連
我々は、TISCH データベースを使用して、OS 内の腫瘍微小環境関連細胞における TERT および IL2RA 遺伝子の発現レベルの解析を実施しました。 我々の発見は、IL2RAがcDC1、単球、およびM2細胞においてより高いレベルの浸潤を示すことを実証した(図1)。 10)。
リスクモデルに関連する遺伝子は、腫瘍微小環境に関連する細胞で発現されました。 OS 微環境関連細胞における TERT (A) および IL2RA (B) の発現レベルは、データセット GSE162454 のヒートマップを使用して視覚化されました。
予後モデルには転移性 OS 患者を区別する機能がある
図に示すように。 11A、高リスク群(TARGET、58.54%、GSE21257、17.25%)と比較して、低リスク群ではより多くの転移なし症例(TARGET、90.25%、GSE21257、58.34%)が観察されました。 さらに、転移性グループと比較して、非転移性グループではリスクスコアが低かった(p < 0.01、図1)。 11紀元前)。 さらに、ROC解析の結果、転移予測における予後モデルの診断性能は、TARGETで0.659、GSE21257で0.705であることが示された(図1)。 11D、E)。 これらの発見は、リスクモデルが OS 患者の転移を予測できることを示しました。
OS患者の転移を予測する予後モデルの能力の評価。 (A) 低リスク群と高リスク群における転移がある場合と転移がない場合の比較。 (B) 転移性グループと非転移性グループのリスク スコアの比較。 (C) OS 転移の予測における診断性能のための ROC 分析。
#免疫細胞浸潤に関連する分子サブタイプと遺伝子サインは骨肉腫患者の予後を予測する